ニュース
キヤノンITS、製薬企業向け「PVLink Report Manager Cloud」を提供
2021/08/24 15:40
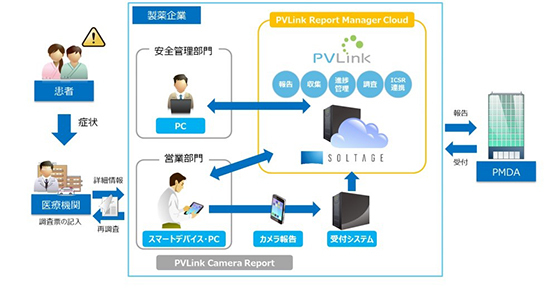
製薬企業は、医薬品の副作用と疑われる症例を確認した場合、厚生労働省所轄の医薬品医療機器総合機構(PMDA)に報告する義務がある。2020年度の「PMDAに対する医薬品の副作用等報告数」は約65万件あり、膨大な症例情報の収集と評価を行う製薬企業の安全管理部門で業務効率化と負荷軽減のため安全性情報進捗管理システムの導入ニーズが高まっている。
しかし、症例情報の収集項目は取扱商品ごとに多岐にわたり、個社に合わせて要件定義を行うシステム開発では、導入までに時間がかかることが問題だった。また、製薬企業のシステム構築では、開発プロセスの検証と文書化がガイドラインとして定められており、初期導入時はもとより、取扱商品の拡大による項目の追加・修正など改修を行うたびに、対応が必要となる。そのため、製薬企業が自社でシステムを開発し、維持管理・運用することは大きな負荷となっている。
こうした製薬企業の課題を解決するため今回、キヤノンITSは製薬企業の安全性情報の進捗管理に必要な機能を標準化し、自社クラウドサービス「SOLTAGE」を活用したPVLink Report Manager Cloudの提供を開始する。
PVLink Report Manager Cloudは、報告・収集・進捗管理・調査・個別症例安全性報告(ICSR)連携など安全性情報管理業務に必要な機能を一式備えており、要件定義にかかる時間を短縮できるため、短期間での導入が可能。さらに、標準の収集項目だけでなく、取扱薬品に特化した個社特有の収集項目も追加することができ、入力必須指定などきめ細かな設定機能を備えている。また、ガイドラインへの対応はキヤノンITSが行い、システムの導入から保守サポートまでワンストップで提供し、顧客の負担を軽減する。
税別価格は、PVLink Report Manager Cloudが初期費用+月額100万円から、PVLink Report Manager(買取型)が初期費用+900万円から。
キヤノンITSは、EDIシステム「EDI-Master DEX for Medical」を製薬企業向けソリューションとして提供しており、これまでPMDAに対する副作用報告の情報を送信する仕組みとして、大手製薬企業で多数の導入実績がある。今後も製薬企業の副作用報告やそれに伴う関連業務についてトータルなソリューションを展開し、製薬企業の顧客の安全性情報管理業務の運用をサポートしていく。
- 1
関連記事
インターネットEDI移行を加速、キヤノンITSとインテックが共同プロモーション
キヤノンITソリューションズ EDI移行の最後の追い込み メニュー刷新、販売パートナーと連携強化
キヤノンITS、「EDI-Masterシリーズ」のラインアップを刷新